ဂျာမေနီယမ်
ဂျာမေနီယမ် သည် အက်တမ်နံပတ် ၃၂၊ သင်္ကေတ Ge ရှိသော ဒြပ်စင်ဖြစ်ပြီး ကာဗွန်အုပ်စုတွင် ပါဝင်သည်။ ဓာတုသဘောအားဖြင့် ဆီလီကွန်အုပ်စုနှင့် ဆင်တူသည်။ သန့်စင်သော ဂျာမေနီယမ်သည် ဆီလီကွန်ကဲ့သို့သော တစ်ပိုင်းလျပ်ကူးဖြစ်သည်။ သဘာဝအားဖြင့် ဂျာမေနီယမ်သည် အောက်ဆီဂျင်နှင့် ဓာတ်ပြုသည်။ သိပ်သည်းဆ မြင့်မားသောနေရာတွင် တွေ့ရှိရသောကြောင့် ဂျာမေနီယမ်အား နောက်ကျပြီးမှ ရှာဖွေတွေ့ရှိခဲ့သည်။
 A 12 gram (2×3 cm) polycrystalline block of germanium with uneven cleaved surfaces | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ယေဘုယျ ဂုဏ်သတ္တိများ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| အမည်၊ သင်္ကေတ | ဂျာမန်နီယမ်, Ge | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အသံထွက် | /dʒərˈmeɪniəm/ jər-MAY-nee-əm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အဆင်း | grayish-white | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင်အလှည့်ကျဇယားရှိ ဂျာမန်နီယမ် | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တမ် အမှတ်စဉ် (Z) | 32 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အုပ်စု၊ ဘလော့ | group 14 (carbon group), p-block | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင်အလှည့်ကျဇယား | period 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဒြပ်စင် ကဏ္ဍ | metalloid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| စံ အက်တောမစ် အလေးချိန် (±) (Ar) | 72.630(8)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အီလက်ထရွန် ပြုပြင်မှု | [Ar] 3d10 4s2 4p2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အခွံတစ်ခုလျင် အီလက်ထရွန်ပါဝင်မှု | 2, 8, 18, 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ရုပ်ပိုင်းဆိုင်ရာ ဂုဏ်သတ္တိများ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဖေ့စ် | အစိုင်အခဲ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အရည်ပျော်မှတ် | 1211.40 K (938.25 °C, 1720.85 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အရည်ဆူမှတ် | 3106 K (2833 °C, 5131 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သိပ်သည်းမှု (အခန်းအပူချိန်) | 5.323 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5.60 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဖျူးရှင်းအပူ | 36.94 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အငွေ့ပျံခြင်း အပူ | 334 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| မိုလာ အပူအင်အား | 23.222 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ငွေ့ရည်ဖိအား
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တောမစ် ဂုဏ်အင်များ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အောက်ဆိုဒ်ဒေးရှင်း အခြေနေ | 4, 3, 2, 1, 0, −1, −2, −3, −4 (an amphoteric oxide) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အီလက်ထရွန် ဆန့်ကျင်ဘက်ဓာတ် | Pauling scale: 2.01 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အိုင်ယွန်းပြုခြင်းစွမ်းအင် | 1st: 762 kJ/mol 2nd: 1537.5 kJ/mol 3rd: 3302.1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အက်တောမစ် အချင်းဝက် | empirical: 122 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ကိုဗေးလန့်အချင်းဝက် | 122 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ဗန်ဒါဝေါ့စ် အချင်းဝက် | 211 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscellanea | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ပုံဆောင်ခဲ ဖွဲ့စည်းပုံ | face-centered diamond-cubic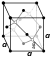 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အသံ၏အမြန်နှုန်း | 5400 m/s (at 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အပူ ပြန့်ကားမှု | 6.0 µm/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အပူစီးကူးမှု | 60.2 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| လျှပ်စစ် ခုခံမှု | 1 Ω·m (at 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Band gap | 0.67 eV (at 300 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သံလိုက်ဓာတ် | diamagnetic[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သံလိုက် ထိတွေ့နိုင်မှု (χmol) | −76.84·10−6 cm3/mol[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young's modulus | 103 GPa[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 41 GPa[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bulk modulus | 75 GPa[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ပိုင်ဆွန် အချိုး | 0.26[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs hardness | 6.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Number | 7440-56-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| သမိုင်းကြောင်း | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| အမည်တပ်ခြင်း | ရှာဖွေတွေ့ရှိမှု ဂျမနီနိုင်ငံအား ကိုယ်စားပြု၍ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ကြိုတင်ဟောခြင်း | Dmitri Mendeleev (၁၈၇၁) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ရှာဖွေတွေ့ရှိမှု | Clemens Winkler (၁၈၈၆) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Most stable isotopes of ဂျာမန်နီယမ် | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
သန့်စင်သော ဂျာမေနီယမ် Germanium သည် ကြွပ်ဆတ်သော အဖြူရောင်သမ်းနေသည့် metalloid ဖြစ်ပါသည်။ ဖွဲ့စည်းပုံမှာ စိန်နှင့် တူနေပြီး ရုပ်ဂုဏ်သတ္တိ၊ ဓာတ်ဂုဏ်သတ္တိတို့တွင် ဆီလီကွန်နှင့် တူနေပါသည်။ ဂျာမေနီယမ်သည် လေထုထဲနှင့် ရေထဲတွင် မည်သူနှင့်မျှ ဓာတ်မပြုပဲ တည်မြဲသောပုံစံနှင့် နေနိုင်ပြီး နိုက်ထရစ်အက်ဆစ် မှလွဲပြီးမည်သည့် အက်ဆစ်တွင်မှ ဂျာမေနီယမ်အပေါ် သက်ရောက်နိုင်ခြင်း မရှိပါ။
အသုံးပြုခြင်း
ဂျာမေနီယမ်သည် အရေးကြီးသော တစ်ပိုင်းလျှပ်ကူးပစ္စည်းဖြစ်ပြီး ထရန်စစ်စတာ (Tarnsistor) နှင့် ဆားကစ်ပြားများတွင် အဓိကအသုံးပြုပါသည်။ ထရန်စစ်စတာများ ဆားကစ်ပြားများတွင် ဂျာမေနီယမ်ကို အဓိကထားပြီး အာဆဲနစ်၊ ဂယ်လီယမ် နှင့် အခြားသတ္တုများကို အနည်းငယ်စီ ရောစပ်ပြီး ပြုလုပ်ထားခြင်း ဖြစ်ပါသည်။ ဂျာမေနီယမ်ကို အခြားသော ဒြပ်ပေါင်းများ ပြုလုပ်ရာတွင်လည်း အသုံးပြုသည်။ ဂျာမေနီယမ် အောက်ဆိုဒ်ကို အလင်းယိုင်ညွန်းကိန်း တိုးမြင့်စေရန် ဖန်ထဲသို့ ပေါင်းထည့်ပါသည်။ သန့်စင်သော ဂျာမေနီယမ်ဖြင့် ပြုလုပ်ထားသော ရေဒီယိုသတ္တုကြွခြင်း (Radiation) စမ်းသပ်ကိရိယာများသည် တိကျစွာ စမ်းသပ်နိုင်သောကြောင့် ၎င်းကိုရိယာများကို လေဆိပ်လုံခြုံရေးတွင် အထူးအသုံးပြုကြပါသည်။ ဂျာမေနီယမ်သည် သံဖြူနှင့် ခဲ တို့လောက်ပင် သဘာဝတွင် ပေါများခြင်းမရှိပါ။ ဂျာမေနီယမ်ကို သဘာဝတွင်းထွက် အနေဖြင့် အနည်းငယ်မျှသာ ထုတ်နိုင်သည့်အတွက် ထုတ်လုပ်မှု ပမာဏနည်းနေခြင်း ဖြစ်ပါသည်။ ဂျာမေနီယမ် အရိုင်းတုံးများသည် အလွန်ကိုရှားပါးပါသည်။ copper-iron-germanium sulfide (germanite) သည် ရှားပါးသောဂျာမေနီယမ် အရိုင်းတုံး ဖြစ်ပြီး ရှာပါးစွာ တူးဖော်ရရှိပါသည်။
ကျန်းမာရေးဆိုင်ရာ သက်ရောက်မှုများ
ဂျာမေနီယမ်ကို နေ့စဉ်တစ်မီလီဂရမ် စားသုံးသင့်ပါသည်။ ဂျာမေနီယမ်ကို သိပ္ပံနည်းကျ သက်သေပြနိုင်မှု မရှိသေးသော်လည်း လူ့ကျန်းမားရေးကို ကောင်းကျိုး ဖြစ်ထွန်းစေနိုင်ပါသည်။ ဂျာမေနီယမ်သည် လူ့ခန္ဓာကိုယ် အတွက် အောက်ဆီဂျင် ရယူရာတွင်လည်း များစွာအထောက်အကူပေးနိုင်ပြီး လူ့ကျန်းမာရေး ကိုလည်း ပိုမိုကောင်းမွန်စေပါသည်။ နောက်ပြီးဆိုးကျိုးဖြစ်စေသော free radicals များကိုလည်း ချေဖျက်ပေးပါသည်။ ဂျာမေနီယမ်သည် သုံးစွဲသူကို ဓာတ်ရောင်ခြည်သင့်ခြင်းမှ ကာကွယ်ပေးပါသည်။ Germaniumhydride နှင့် germaniumtetrahydride တို့သည် မီးလောက်လွယ်ပါသည်။ လေနှင့်တွေ့လျှင် ပေါက်ကွဲ စေနိုင်ပါသည်။ ရှူရှိုက်မိပါက ဗိုက်နာခြင်း၊ ချောင်ဆိုးခြင်း၊ အရေပြားနာကျင်ယားယံခြင်း၊ မျက်စိအောင့်ခြင်း တို့ဖြစ်စေနိုင်ပါသည်။
ပတ်ဝန်းကျင်သို့သက်ရောက်မှုများ
လေထုထက် ပိုမိုလေးလံသောကြောင့် မြေပြင်တွင် ပျံ့နှံ့တည်ရှိနေပါသည်။[5]
ကိုးကား
- Standard Atomic Weights 2013. Commission on Isotopic Abundances and Atomic Weights
- Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics 81st edition, CRC press.
- Weast၊ Robert (1984)။ CRC, Handbook of Chemistry and Physics။ Boca Raton, Florida: Chemical Rubber Company Publishing။ pp. E110။ ISBN 0-8493-0464-4။
- "Properties of Germanium"၊ Ioffe Institute]။
- ဒြပ်စင်အလှည့်ကျဇယား ဘာသာပြန်ဆိုမှု ပရောဂျက်တွင် ပါဝင်သူ ကိုတင်ကျော်ဦး ဘာသာပြန်ဆိုသည်။